北海道大学大学院先端生命科学研究院の西村紳一郎特任教授と北海道大学発創薬ベンチャーの遠友ファーマ株式会社(本社:札幌市、代表取締役CEO:安井忠良)の研究グループは、これまで抗接着性の「ナノソーム」という粒径20~50ナノメートル程度の超高性能ナノ微粒子を利用したがん治療用ナノ医薬(nanomedicine)の基礎的な研究を進めてきました(例えば、J. Am. Chem. Soc. 2011, 133, 12507-12517; ACS Chem. Biol. 2015, 10, 2073-2086; Angew. Chem. Int. Ed. 2019, 58, 14513-14518; Biomaterials 2022, 280, 121314; Adv. NanoBiomed. Res. 2023, 2300076など)。今回本研究グループは、がんの中でも最も致死率の高い難治性のがんとされる膵臓がん(膵がん)の画期的な治療法の実現が期待できる革新的なナノ医薬の開発に成功しました。
膵がんは早期発見が極めて困難で、見つかった時には既にがん細胞が浸潤や転移を起こしていることが多く、また大きな効果が期待できる治療法がほとんどないため患者の5年生存率は10%以下の難治性がんです。膵がんに限らず、がん特異的な標的分子が中々見つからないことが、これまで有効性の高い治療薬の開発が実現していない大きな理由の一つとなっています。今回、西村特任教授の研究グループは、正常細胞では細胞内のリソソームに局在している「ノイラミニダーゼ-1(NEU-1)」が多くのがんで細胞膜の表面にも発現していることに着目して、ナノソームから膵がん細胞膜のNEU-1を標的とする「ナノソーマルイリノテカン(Nanosomal Irinotecan)」を設計しました。
具体的にはナノソームの表面にNEU-1を標的とする「非可逆的阻害剤」と細胞内のDNAトポイソメラーゼ阻害剤のイリノテカンを同時に搭載させることで、抗がん剤を膵がん細胞のみに届ける方法である「能動的薬物送達システム(Active Drug Delivery System, Active DDS)」が初めて実現しました。ナノソーマルイリノテカンをヒト膵がん細胞と共培養したところ、膵がん細胞膜に特異的に発現するNEU-1を介して搭載した抗がん剤のイリノテカンを膵がん細胞内のみに届けることに初めて成功し、低濃度のナノ医薬(IC50=8.07 nM)が膵がん細胞を培養開始後24時間で完全に死滅させることを証明しました。
さらに、ヒト膵がん細胞塊を移植したマウスにこのナノ医薬(5 mg/kg)を4日間隔で6回静脈内投与した結果、移植した膵がん細胞塊の成長は完全に阻止されること、またこの治療期間内において副作用によるマウスの体重減少が全く認められないことが示されました。
なお、本研究成果は、2025年7月22日(火)公開のAdvanced Healthcare Materials誌にオンライン掲載されました。
【ポイント】
- 膵臓がん細胞の表面に特異的に発現する酵素NEU-1を標的とする革新的ナノ医薬を開発。
- ヒトの膵臓がん細胞塊を移植したマウスを用いた動物実験により、高い治療効果と安全性を証明。
- がん細胞のみに取り込まれるナノ医薬による副作用の低い効果的な膵臓がん治療法の実現に期待。
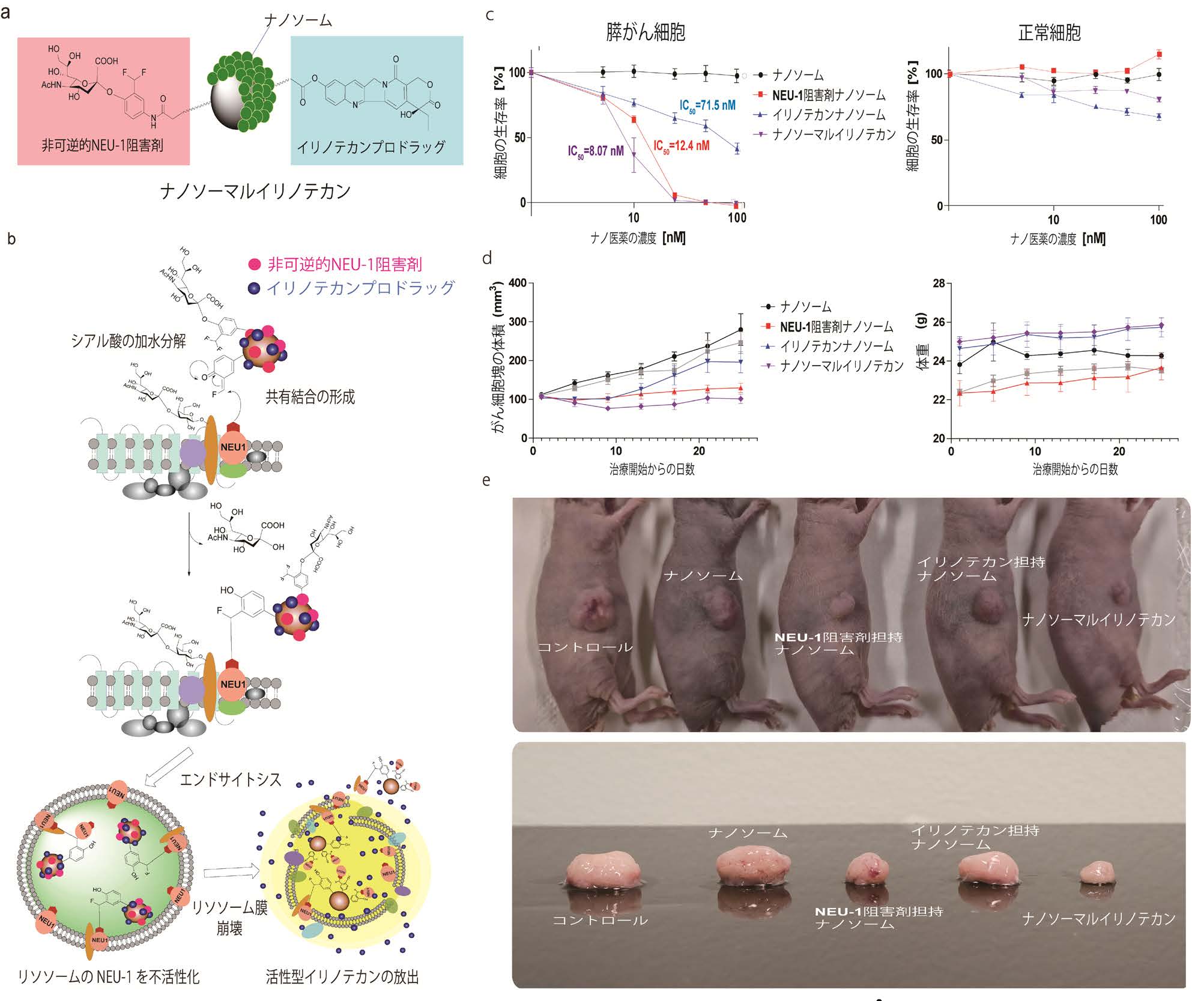
a) ナノソーマルイリノテカンの化学構造、b) ナノソーマルイリノテカンによる抗がん活性の作用メカニズム、c) ナノソーマルイリノテカンのがん特異的細胞障害活性、d) 膵がん細胞塊移植マウスに対するナノソーマルイリノテカン及び比較ナノソームの抗がん活性と安全性(正常細胞に対する副作用)、 e) ナノソーマルイリノテカン及び比較ナノソームによる24日間の治療後の移植した膵がん細胞塊の様子
プレスリリース:膵臓がんの画期的なナノ治療薬の開発に成功!~がん細胞のみに抗がん剤を届ける副作用の低い能動的薬物送達システムを初めて実現~(先端生命科学研究院 特任教授 西村紳一郎)